Introducción
Las enfermedades infecciosas en pacientes con supresión inmunológica avanzada, ya sea causada por cirugías, co-infecciones virales, HIV o exposición ambiental suelen ser difíciles de manejar, con un claro impacto tanto en el tiempo de estadía hospitalaria como en el tratamiento y los resultados clínicos finales. Las infecciones por Cándida spp y Aspergillus spp son las causas más frecuentes de micosis invasivas. Los métodos de diagnóstico más usados son el hemocultivo y las técnicas basadas en el sistema antígeno-anticuerpo, pero aun así son subóptimos, llevando a retrasos en el inicio de las terapias antifúngicas. Esto tiene como consecuencia que a pesar de contarse con varios antifúngicos de última generación, los índices de mortalidad siguen siendo muy elevados(1,2,3,4,5,6,7).
El diseño y desarrollo de nuevos radiofármacos para centellografía de infecciones está basado en la definición y descripción de las propiedades ideales para esta categoría. Estos compuestos deben tener alta sensibilidad para infección/ inflamación y capacidad de diferenciar entre infección aguda y crónica. Asimismo deben tener alta especificidad, rápida depuración sanguínea y escasa captación gastrointestinal. Por último deben ser fáciles de preparar, económicos y fácilmente asequibles. Se ha trabajado mucho en estas líneas y es así que algunas mejoras importantes en las técnicas nucleares SPECT y PET para detectar infecciones incluyen el radiomarcado de antifúngicos, antibióticos, anticuerpos monoclonales, péptidos quemotácticos, liposomas y agentes mediados por avidina. Entre los agentes antimicrobianos que pueden ser radiomarcados se encuentran los grupos de antifúngicos como azoles, equinocandinas y anfotericina; estos pueden ser marcados con un agente emisor gamma que permita la detección de los focos de infección(8,9,10,11,12).
En este trabajo se realizó un estudio comparativo del comportamiento fisicoquímico y biológico de los complejos radiomarcados de los antifúngicos fluconazol y voriconazol como potenciales agentes para el diagnóstico de infecciones mediante centellografía gamma.
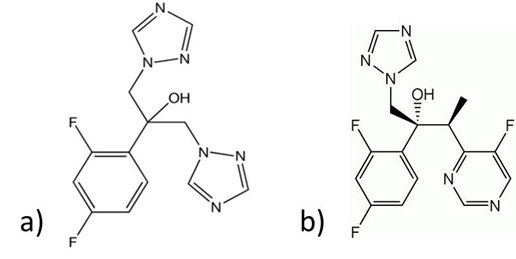
El fluconazol (F) es un antifúngico ampliamente utilizado. Como otros triazoles, tiene 2 anillos conteniendo 3 átomos de nitrógeno; el anillo bencénico a su vez posee 2 átomos de flúor (fig. 1a). Su estructura simétrica y polar favorece la hidrosolubilidad; es una base extremadamente débil (pKa 3,7) y no es ionizable a pH fisiológico. Su forma de acción es a través de la inhibición de la enzima citocromo P45014α-demetilasa, requerida para la síntesis del ergosterol; esta enzima es fundamental para la producción y mantenimiento de la pared celular fúngica. El fluconazol puede asociarse a los sitios activos de la enzima mediante enlaces de hidrógeno entre su grupo OH y el grupo C=O de la enzima.
El voriconazol (V) es un antifúngico de amplio espectro generalmente utilizado para el tratamiento de infecciones severas en pacientes inmunocomprometidos. Se trata de un triazol de segunda generación, que inhibe la enzima citocromo P450 14α-demethylasa (fig. 1b)(13,14,15,16).
Dado que ambos antifúngicos cuentan con aminas aromáticas, son capaces de unirse al complejo precursor fac-[99mTc][(CO)3(H2O)3]+, el cual es ampliamente utilizado debido a sus ventajas de fácil preparación y estabilidad química.
El triaquotricarboniltecnecio(I) fac-[99mTc][(CO)3(H2O)3]+ es un complejo desarrollado por Alberto et al(17), que puede ser utilizado como precursor de una variedad importante del compuestos. Este precursor cuenta con 3 posiciones de coordinación ocupadas por moléculas de CO fuertemente unidas al metal. El intenso campo ligando resultante, conjuntamente con la configuración electrónica d6 de bajo spin del metal, favorece el estado de oxidación +1 y previene que ocurran otras reacciones de oxidación-reducción. El resto de las posiciones de coordinación está ocupado por 3 moléculas de agua débilmente unidas, las que pueden reemplazadas por átomos donores con gran afinidad por el metal. Existe una gama amplia de posibilidades, desde grupos duros e hidrofílicos basados en ácidos carboxílicos y aminas alifáticas, hasta otros blandos y lipofílicos, preferentemente aminas aromáticas. La ventaja de este tipo de core radica en que las tres posiciones que quedan libres para la sustituciónse pueden coordinar con varios ligandos (mono, bi o tridentados) formando distintos tipos de conjugados. La síntesis de los complejos tricarbonílicos de fluconazol y voriconazol puede realizarse mediante la sustitución directa de moléculas de agua del precursor por los ligandos de interés(17,18,19,20,21,22,23,24,25).