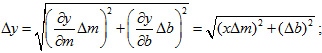Materiales y método
Bases teóricas (sensibilidad)
La eficiencia o sensibilidad S de detección de un detector está, en general, dada por(3):
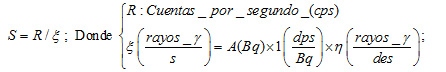
Aparte de esta relación, la eficiencia S depende a la vez de cuatro factores, a saber, la eficiencia geométrica (g), la intrínseca (Ɛ), un factor de absorción y de dispersión (F), y un factor que toma en cuenta la fracción de las señales que salen del detector y caen en la ventana del analizador de pulsos (f); matemáticamente esto se representa como:
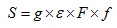
A pesar de ello, se puede simplificar entendiendo la sensibilidad como las cuentas registradas por el detector dividida por los fotones emitidos por la fuente (ver ecuación 3). Esto puede llevarse a cabo manteniendo constantes los parámetros anteriormente especificados. La constancia en la eficiencia geométrica se logra utilizando siempre los mismos tubos para la obtención de las muestras de sangre, que siempre serán de 1 mL, igual al volumen y el tubo utilizado en el estándar. Los otros tres factores se consideran constantes en el tiempo, dado que el contador de pozo y las condiciones externas se mantienen constantes.
El factor ξ en la ecuación 1 que incluye a su vez el factor η (rayos gamma emitidos por cada desintegración) se cubre en su totalidad (todos los fotones) utilizando la actividad inicial de la muestra obtenida de un contador de pozo bien calibrado.
Por lo anterior, podemos dar una definición simplificada de la sensibilidad como:

Como se muestra en la ecuación 4, tanto la sensibilidad para el estándar como para la muestra de sangre se relacionan con sus respectivas cuentas por minuto y sus actividades de la siguiente forma:
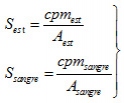
Además, considerando una constancia en la sensibilidad geométrica y temporal del contador, es decir, Sest = Ssangre, podemos obtener la actividad en sangre como sigue:
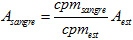
Medida de la actividad y diluciones
Para medir la actividad de la muestra inicial se ha utilizado un activímetro Capintec® modelo CRC-15C. Las sucesivas diluciones se realizaron con una micropipeta Accumax PRO de 100-1000 µCi (para cada medida se cambia el tip) y las mediciones de cps de todas las diluciones se han realizado con un contador de pozo Capintec® modelo Captus-3000. Se utilizaron para todas las diluciones tubos Plain Tube de Vacu Lab® modelo VP900013S de 9,0 mL.
Obtención de la curva de calibración
A partir de un estándar inicial de actividad conocida se obtuvieron sucesivas diluciones. Se mide la actividad de la primera muestra de forma que esta sea mucho mayor que la incertidumbre del contador. Las siguientes muestras se obtienen con la micropipeta extrayendo porcentajes del volumen anterior según se explica más adelante, de forma que la actividad de estas se reduce en proporción igual al volumen. Como se menciona al inicio, cada una de las muestras posee una fracción de la muestra inicial de actividad conocida; la primera dilución se obtiene extrayendo 1/10 de la muestra inicial. En consecuencia, se asume que la actividad de ésta será también 1/10 de la actividad de la muestra inicial. Dado que el volumen de la muestra inicial es de 1 mL, al extraer 1/10 de la misma se obtiene una primera dilución con un volumen de 0,1 mL, al que se le agrega 0,9 mL de tiosulfato para obtener un volumen final de 1 mL. La segunda dilución se obtiene extrayendo un décimo de la primer dilución recién preparada; de igual forma se completa con 9/10 de tiosulfato para completar 1 mL. Nótese que en este último caso, la dilución tiene 1/10 de la actividad de la dilución anterior, lo que equivale a 1/100 de la actividad de la muestra inicial. Este proceso se repite hasta completar 9 diluciones. No en todas las muestras se extrae una fracción de 1/10 del volumen anterior. Las fracciones de volumen extraídas así como los volúmenes de dilución que representan y los volúmenes de tiosulfato que completan un 1 mL de cada una se muestran en la tabla A1 del Apéndice; en la misma también se indica qué fracción de actividad de la muestra inicial posee cada dilución.
A partir de la cuarta dilución, cada una se mide cinco veces en un contador de pozo del que se obtiene las cuentas por minuto (cpm). La curva de calibración se construye entonces graficando para cada muestra de cierta actividad, las cuentas por minuto promedio correspondientes. Los puntos graficados cubren en su intervalo las cuentas que se espera obtener, por lo que una curva de mejor ajuste permite interpolar la actividad de cualquier muestra conociendo sólo la lectura de sus cuentas por minuto.
El siguiente apartado muestra el tratamiento formal que se hizo de la incertidumbre en el proceso completo de obtención de la curva de mejor ajuste y de la consecuente incertidumbre asociada a la actividad de una muestra -calculada a partir de su medida en cpm- con la curva de calibración.
Cálculo de incertidumbres
Ningún experimento en el que se mide cierta magnitud es absolutamente preciso, es decir, el resultado de la medida no coincide con el valor real de la magnitud(4). La diferencia entre el valor real y el valor medido se denomina error de la medida. A pesar de que el error siempre será desconocido, puede estimarse una cota superior para su valor absoluto; esta cota se denomina incertidumbre de la medida. Siendo Xmed el valor medido, Xreal el valor real y ΔX la incertidumbre, matemáticamente lo anterior se resume como:
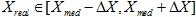
Por lo tanto, una medida siempre se debe reportar como:
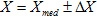
La incertidumbre se calcula de forma diferente dependiendo de si el valor de la magnitud se observa directamente en un instrumento de medida (medida directa) o si se obtiene manipulando matemáticamente una o varias medidas directas (medidas indirectas).
Medidas directas
La incertidumbre vinculada a medidas directas se compone de aquellas incertidumbres asociadas a la precisión finita del instrumento θ y a la incertidumbre asociada a factores ambientales y aleatorios Ψ como lo son vibraciones o pequeños cambios de temperatura. La incertidumbre total se obtiene en cuadratura como 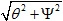 .
.
Las medidas directas realizadas fueron: actividad con un activímetro, volúmenes con una micropipeta y cuentas por minuto con la sonda de captación. Las incertidumbres asociadas al instrumento de medición se presentan en la tabla 1.
| Medición de | Instrumento | Incertidumbre θ |
|---|---|---|
| Volumen | Micropipeta 100-1000 μL | 2,5 μL |
| Actividad | Activímetro | 10 μCi |
| Cuentas | Contador de pozo | √cpm |
La incertidumbre aleatoria afecta a la medida de las cuentas en el contador de pozo, que en nuestro caso se realizó 5 veces para cada dilución. La incertidumbre aleatoria se obtiene como:
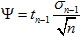
Donde tn-1 es la función t de student y σn-1 la dispersión de las medidas, la que viene dada por:
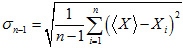
Para 5 medidas n = 5, además tn-1 = t4 = 4,60. Así, aplicando las ecuaciones 8 y 9 a los datos mostrados en la tabla A2 del Apéndice, se obtienen las incertidumbres que allí se muestran. En la penúltima columna de dicha tabla aparece la incertidumbre absoluta, que es la incertidumbre del promedio, la cual se calcula utilizando la ecuación 14 que aparece en el siguiente apartado.
Medidas indirectas
El valor final a obtener es la actividad Ai que hay en un cierto volumen Vi, es decir, la concentración Ci y viene dada por:
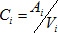
La medida de actividad sólo se realiza para la muestra inicial y es A1 = (2450 ± 10) μCi en un volumen V1 = (1,0000 ± 0,0025)mL ; las diluciones siguientes se obtienen como una fracción Ki de este volumen, de la siguiente forma:
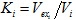
Donde Vex es el volumen extraído del volumen actual, es decir Vi. Como anteriormente se dijo, todo volumen medido es de 1 mL, que es el total del volumen extraído más el volumen de tiosulfato con el que se completa cumpliendo: Vi = Vi-l. Los volúmenes anteriores se definen respectivamente como:
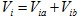
La actividad de la dilución subsiguiente es una fracción de la anterior y vendrá dada por la fracción de volúmenes extraídos (como se aprecia en la ecuación 11), es decir:
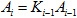
Donde Ki se puede obtener de forma recursiva de la dilución extraída anteriormente de la misma forma que se utiliza Ai-l.
La incertidumbre de una medida indirecta se obtiene de la siguiente forma:
Si tenemos que Y = f (X1,X2,...,XN , entonces su incertidumbre es:
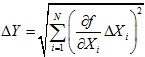
En nuestro caso, se quiere hallar la incertidumbre de la concentración Ci ; utilizando las ecuaciones 10 y 14 obtenemos que:
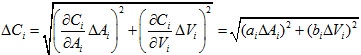
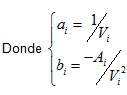
Nótese que en la ecuación 15 aparecen las incertidumbres asociadas a la actividad Ai y al volumen Vi ; estas se obtienen a su vez aplicando la ecuación 14 a las ecuaciones 12 y 13, y posteriormente a la ecuación 11; haciendo esto, se obtiene entonces que:
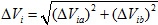
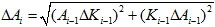
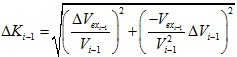
Las incertidumbres asociadas a las medidas indirectas se resumen en la Tabla 2.
| Dilución | Concentración | |||
|---|---|---|---|---|
| Valor (μCi / mL) | ± | Incertidumbres | ||
| Absoluta (μCi / mL) | Relativa % | |||
| 4 | 0,28 | ± | 0,016 | 5,7 |
| 5 | 0,070 | ± | 0,0041 | 5,8 |
| 6 | 0,014 | ± | 0,00084 | 6,0 |
| 7 | 0,0028 | ± | 0,00017 | 6,0 |
| 8 | 0,00056 | ± | 0,000038 | 6,8 |
| 0,00011 | ± | 0,0000077 | 6,9 | |
Recta de mejor ajuste: regresión lineal
Tomando en cuenta lo discutido anteriormente y el cálculo de incertidumbres mostrado, se obtienen finalmente los puntos y la curva de calibración (fig. 1), donde se muestra el ajuste lineal que permite interpolar los valores de concentración para un cierto número de cuentas.
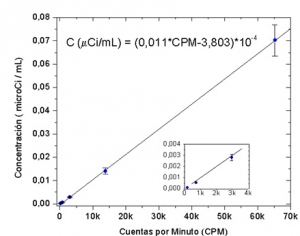
Como se aprecia en la figura, los datos siguen un comportamiento lineal, por lo que se ha decidido ajustarlos por regresión lineal. Este método permite encontrar la ecuación de la línea recta que mejor se ajusta a los datos, es decir una ecuación del tipo:
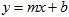
Los requisitos para poder aplicar este método de ajuste son los siguientes:
- La incertidumbre de la variable independiente se considera despreciable.
- Todos los datos de la variable dependiente tienen la misma incertidumbre relativa.
Para el primer requisito, observando en la tabla A2 del Apéndice se puede ver que la incertidumbre relativa en todos los casos es < 4%, por lo que se pude considerar despreciable. Para el segundo requisito, observando la Tabla 2 se puede ver que todas las incertidumbres absolutas son muy parecidas y se ubican alrededor del 6%.
Las ecuaciones que nos permiten obtener tal línea son las siguientes(4):
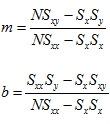
En donde debe entenderse:
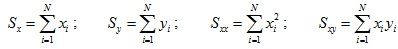
Incertidumbre de la recta de mejor ajuste
De acuerdo con la ecuación 6, cada parámetro de los que aparecen en la ecuación 20 tiene una incertidumbre asociada, de modo tal que la ecuación de la recta debe presentarse según la ecuación 7 de la siguiente forma:
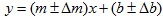
La obtención de la incertidumbre en la pendiente y en la intersección con el eje Y se aprecia de la siguiente forma:
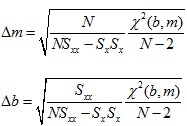
En donde X2 (chi cuadrado) que es una medida de la desviación total de los valores yi respecto a los predichos por el modelo lineal y = mx + b , viene dado por:
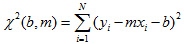
Así, con todo lo anterior finalmente se obtiene la línea de mejor ajuste entre los valores de cuentas por minuto y concentración, como sigue:
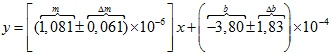
La incertidumbre asociada a la variable dependiente se obtiene aplicando la ecuación 14 y tomando en cuenta que la incertidumbre de la variable independiente es despreciable, se obtiene de la siguiente manera: