Hiperostosis cortical infantil: reporte de un caso y breve descripción de las diferencias clínicas, radiológicas y centellográficas con el maltrato infantil
Karina Quintero Rodriguez1, Romina Lorena Romero2, César Mendez2, Marcelo Cerutti3, Luz Yamila Baez4, María del Carmen Alak2.1 - Servicio de Medicina Nuclear Hospital Nacional de Pediatría Garrahan, Buenos Aires, Argentina..2 - Servicio de Medicina Nuclear Hospital Británico de Buenos Aires, Buenos Aires, Argentina..3 - Servicio de Radiología Hospital Nacional de Pediatría Juan P. Garrahan, Buenos Aires, Argentina..4 - Servicio de Pediatría Hospital de San Justo, San Justo, Provincia de Buenos Aires, Argentina..
Introducción
La hiperostosis cortical infantil o enfermedad de Caffey-Silverman (también llamado síndrome de Caffey) es una entidad clínica caracterizada por neoformación ósea perióstica secundaria a un proceso inflamatorio, con afección de los tejidos blandos circundantes(1). Fue inicialmente descripta por Roske en 1930 y luego caracterizada por Caffey y Silverman en 1945(2). Presenta una incidencia de 48 casos por cada 100.000 recién nacidos vivos(3) y tiene dos formas de presentación: una prenatal (letal) y otra infantil o de los primeros años de vida, ésta última generalmente autolimitada. La mayor parte de los casos son hereditarios y el patrón de herencia para la mutación más estudiada (gen COL1A1, 17q21) es autosómico dominante con penetrancia incompleta(4). La forma prenatal tiene un patrón de herencia autosómico recesivo(1). La enfermedad de Caffey (EC) puede simular una fractura con reacción perióstica excesiva a nivel cortical y debe descartarse (junto con otras enfermedades metabólicas) antes de determinar un diagnóstico de maltrato infantil(5). Es importante, por tanto, conocer su clínica, realizar un correcto diagnóstico diferencial con otras patologías superponibles en cuanto a sintomatología y conocer su historia natural, para poder diagnosticarla y tratarla de forma adecuada. El objetivo es presentar un caso de esta colagenopatía poco frecuente, que se benefició de los hallazgos centellográficos iniciales para arribar al diagnóstico.
Descripción del caso
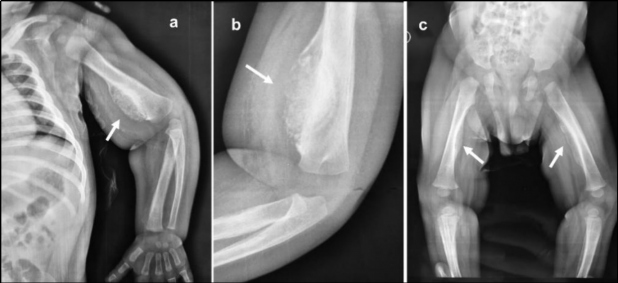
Paciente de 7 meses, sin antecedentes patológicos, traído a la consulta por dolor a la movilización del miembro superior izquierdo, de 5 días de evolución. Madre de oficio boxeadora profesional. Al examen físico se evidencia tumoración local en miembro superior izquierdo, sin signos inflamatorios y con movilidad disminuida, sin otra alteración evidente. Se realizan radiografías de miembros superiores e inferiores que muestran lesiones óseas (Fig. 1), por lo que se decide su internación por sospecha inicial de maltrato infantil.
El laboratorio demostró hemograma de bajo riesgo, sin atipias celulares en frotis de sangre periférica; función renal, hepática y perfil lipídico normales, sin alteración de electrolitos ni LDH y perfil fosfo-cálcico normal. La ecografía abdómino-renal y la valoración cardiológica fueron normales.
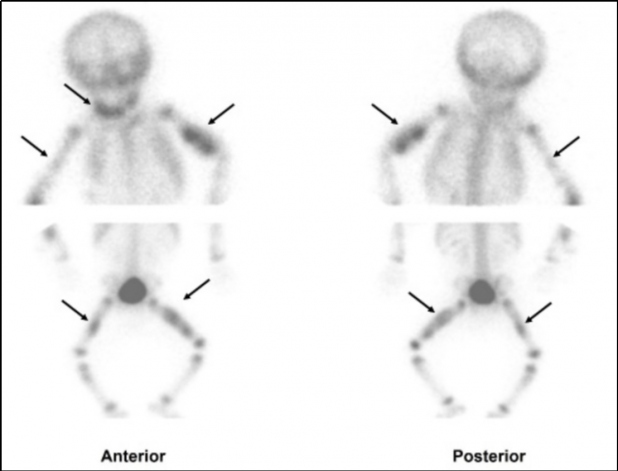
El centellograma óseo mostró áreas de concentración anómala del trazador en maxilar inferior derecho, húmero izquierdo, fémur ipsilateral y, con menor intensidad, en fémur derecho así como distribución irregular en húmero derecho (Fig. 2).
Debido al hallazgo de captación anómala a nivel mandibular se arribó a la presunción diagnóstica de EC, realizándose biopsia del húmero izquierdo que informó hueso reticular neoformado con reborde osteoblástico y médula fibrovascular sin atipia celular, cuadro histológico compatible con hiperostosis cortical infantil.
Discusión
La EC se caracteriza por un crecimiento subperióstico masivo que afecta a la diáfisis de huesos largos, así como a costillas, mandíbula, escápula y clavículas. La forma de presentación más habitual se caracteriza por la aparición de picos febriles sin claro foco, edema de partes blandas, irritabilidad y dolor en lactantes, debiendo considerarse causas infecciosas y no infecciosas. Lo más frecuente es que la clínica se desarrolle entre el quinto y séptimo mes de vida, aunque puede presentarse a partir de la novena semana de vida; no se ha descrito predilección por un género. La historia natural de la enfermedad ha demostrado que la evolución es autolimitada(2).
Existen muy pocos casos descritos en la literatura, y debido a su autolimitación se considera una patología subdiagnosticada, ya que su manifestación clínica es muy inespecífica. Existen dos formas de presentación(5,6): 1) La forma clásica infantil, cuya afectación suele ser asimétrica. La zona más afectada suele ser la mandíbula (70-90% de los casos), lo cual habitualmente se utiliza como criterio diagnóstico. En la mitad de los casos existe afectación clavicular, y en un 20-30% se objetiva afectación de costillas y escápulas. Tanto la epífisis como la metáfisis de los huesos largos suelen estar libres de la enfermedad. Tras la fase aguda, que tiene una duración de 1-2 semanas, le sigue una fase subaguda asintomática con cambios radiológicos (reacción subperióstica e hiperostosis con deformidades secundarias o sin ellas) que suelen persistir meses o años hasta la resolución completa sin secuelas. También es posible la recidiva(7) dando paso a una fase crónica, que rara vez deja secuelas definitivas (deformidad, acortamiento, etc.) y finaliza antes de los 2-3 años(8). Los cambios radiológicos son característicos, desarrollándose habitualmente en las tres primeras semanas. 2) La forma prenatal, más severa y mucho menos frecuente. Se caracteriza por hiperostosis ósea más extendida que en la forma clásica, angulación y acortamiento de huesos largos, polihidramnios e hidrops fetal. Este subtipo está relacionado con un alto índice de mortalidad en relación con prematuridad e hipoplasia pulmonar(5,6).
El desarrollo de la EC puede ser esporádico (por mutación de novo) o transmitirse de forma autosómica dominante mediante penetrancia incompleta. En los casos de afectación familiar, se ha identificado una mutación en el exón 41 (substitución de arginina por cisteína), que codifica la cadena 1 de colágeno tipo I (gen COL1A1). Este gen es responsable de otras enfermedades del colágeno como la osteogénesis imperfecta o el síndrome Ehlers-Danlos. En el caso del subtipo prenatal, al parecer la transmisión se produce de forma recesiva(4,5).
Ante la sospecha de un caso de EC, es muy importante realizar un correcto diagnóstico diferencial con otras enfermedades que cursen con inflamación ósea como osteomielitis (la entidad más difícil de diferenciar en la fase aguda), hipervitaminosis A, escorbuto, tumores óseos y maltrato (Tabla 1)(8).
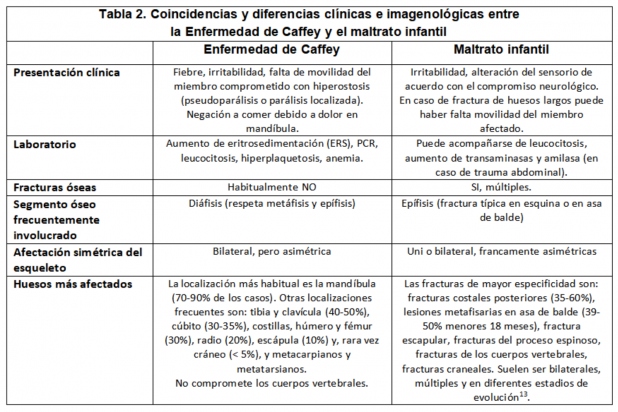
La EC y las enfermedades metabólicas son diagnósticos muy poco comunes entre los niños evaluados por sospecha de abuso. Por ejemplo, en un estudio observacional prospectivo de 2890 niños sometidos a evaluación por maltrato físico, solo 19 tenían enfermedad ósea metabólica, incluida deficiencia de vitamina D, osteoporosis, hiperparatiroidismo y síndrome de Menkes(8). Diferenciar una enfermedad ósea metabólica del maltrato infantil requiere de un examen clínico, radiológico y de laboratorio adecuado (Tabla 2). Sin embargo, la presencia de enfermedad ósea metabólica no excluye la posibilidad de abuso infantil concomitante, una coincidencia rara, pero posible. Dado que el diagnóstico de maltrato exige una intervención legal sobre el entorno del menor involucrado, es sumamente importante descartar otras causas, antes de proceder a la separación de sus padres o tutores (sospechados de perpetrar el maltrato).
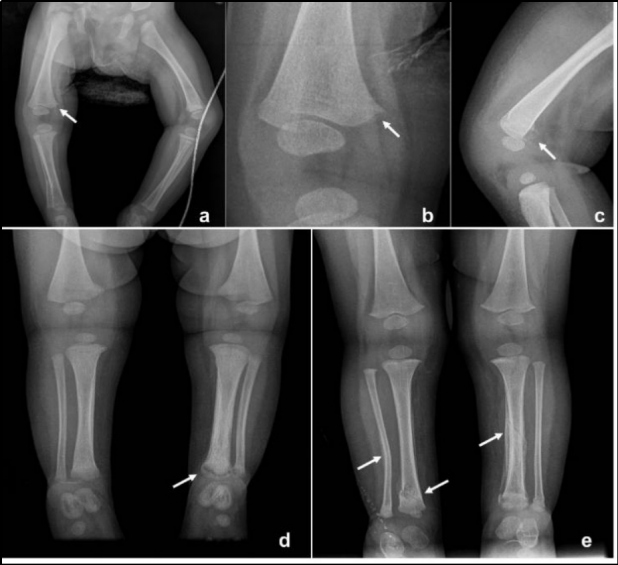
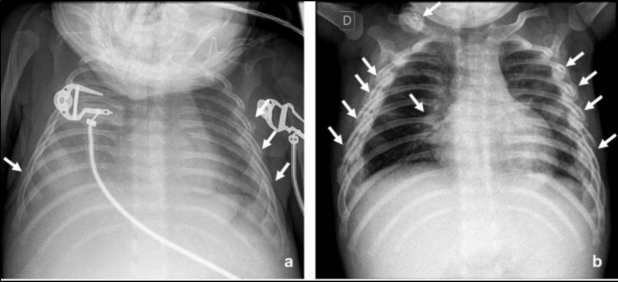
Se consideran fracturas altamente específicas de maltrato físico las costales posteriores y la lesión metafisaria clásica (fractura en esquina y en asa de balde) (Fig. 3)(10,14). Las fracturas costales en lactantes y niños pequeños se han relacionado con maltrato hasta en el 82% de los casos(11). En niños menores de 3 años, el valor predictivo positivo de las fracturas costales como indicador de maltrato es de un 95%(12).
En lactantes fallecidos por maltrato físico, las fracturas más comunes son las costales(13), que en ocasiones no son evidentes en la radiografía por no haber aún desarrollado reacción perióstica y callo óseo (Fig. 4) (13,14,15).
En lactantes o niños menores de 2 años con fracturas de huesos largos, la radiografía esquelética identifica fracturas adicionales hasta en un 10% de los casos(15). Precisar el tiempo de evolución de las fracturas es fundamental en la evaluación radiológica del maltrato. La formación de hueso subperióstico ocurre generalmente entre los 7 y 10 días; el callo blando se ve entre los 10 y los 14 días y la formación de callo duro entre los 14 y 21 días(10). Cuando el patrón de curación no concuerda con la historia aportada por los adultos, se debería considerar la posibilidad de maltrato (13,15).
Cuando el estudio radiológico esquelético es normal o ambiguo y existe alta sospecha de maltrato, puede realizarse una gammagrafía ósea (como lo afirma el panel de expertos de American College of Radiology, ACR: “Indicado cuando la sospecha clínica de abuso sigue siendo alta y todavía es necesaria la documentación” )(15).
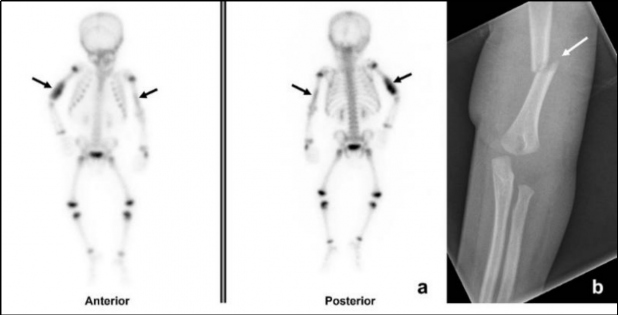
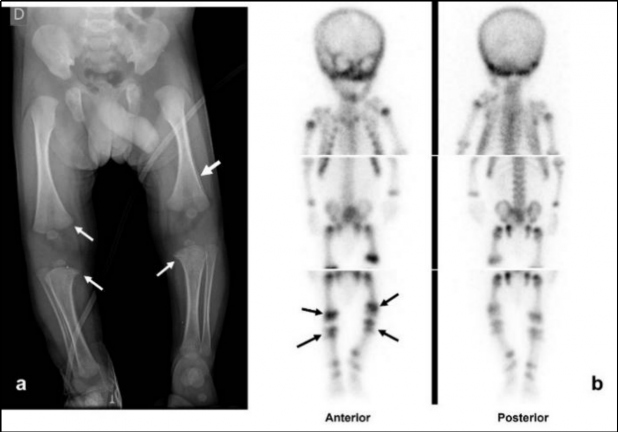
El centellograma óseo también puede realizarse como una alternativa a la seriada esquelética en niños entre 2 y 5 años, ya que la probabilidad de lesión metafisaria clásica es baja en este grupo de edad (Fig. 5). Conway et al. y otros, en un informe de dos estudios y una revisión de la literatura, concluyen que la gammagrafía esquelética es el mejor estudio complementario para la evaluación de la sospecha de abuso infantil(13). La gammagrafía puede identificar fracturas agudas de costillas que no son evidentes en las radiografías, pero es menos sensible en la detección de las fracturas metafisarias (Fig. 6) y fracturas de cráneo (13,16).
Habitualmente en nuestras instituciones el centellograma esquelético se realiza sin anestesia; se intenta privar antes al niño de sueño, indicándole a la persona cuidadora que lo haga conciliar el sueño inmediatamente antes de adquirir las imágenes. El estudio es de gran utilidad ya que los cambios metabólicos preceden a los anatómicos, visualizándose las fracturas aun cuando estas no presenten signos de reparación radiográfica, así como también la distribución y extensión de las lesiones. En nuestro caso fue útil al permitir identificar el compromiso mandibular no detectado en el examen físico ni radiológico inicial.
En conclusión, el diagnóstico de la EC es un desafío, debido a las similitudes que guarda con otras enfermedades metabólicas y con el maltrato. Una rigurosa técnica radiológica, así como el análisis exhaustivo de las imágenes (incluido el centellograma óseo como primer estudio a solicitar en forma complementaria), en conjunto con el historial clínico y las pruebas de laboratorio, resultan fundamentales para establecer un diagnóstico preciso. La EC suele tener un curso autolimitado y el manejo es conservador; por lo tanto, se deben conocer sus características para arribar a un diagnóstico correcto y tranquilizar a los padres sin tomar medidas drásticas en relación a la exclusión del niño de su entorno familiar, como sería el caso en el maltrato.
Referencias
- Nemec SF, Rimoin DL, Lachman RS. Radiological aspects of prenatal onset cortical hiperostosis. Eur J Radiol 2012; 81:565-657.
- Caffey J, Silverman W. Infantile cortical hyperostosis, preliminary report of a new syndrome. Am J Roentgenol Rad Therapy 1945; 54:1-16.
- Gurruchaga Gutiérrez I, Cutillas Ruiz R. Síndrome de Caffey-Silverman. Rehabilitación (Madr), 2017; 51:57-60.
- Nistala H, Mäktie O, Jüppner H. Caffey disease: new perspectives on old questions. Bone 2014; 60:246-251.
- Rodríguez M, Martínez LE, Cortés J, et al. Hiperostosis cortical infantil: reporte de caso. Revista Chilena de Pediatría 2016; 87:401-5.
- Kamoun-Goldrat A, Le Merrer M. Infantile cortical hyperostosis (Caffey disease): A review. J Oral Maxillofac Surg 2008; 66:2145-50.
- Navarre P, Pehlivanov I, Morin B. Recurrence of infantile cortical hyperostosis: A case report and review of the literature. J Pediatr Orthop 2013; 33:e10-e17.
- Lee DY, Kim WJ, Kim B, et al. Differential diagnosis between child abuse and infantile cortical hyperostosis: A case report and literature review. Int J Environ Res Public Health 2021; 18:12269.
- Almeida JFL, Kimura H, Hercowitz LH, et al. Cortical hyperostosis secondary to prolonged use of prostaglandin E1. Clinics 2007; 62:363-6.
- Delgado Álvarez I, Barber Martínez de la Torre I, Vázquez Méndez E. El papel del radiólogo ante el niño maltratado. Protocolo de imagen y diagnóstico diferencial. Radiología 2016; 58(S2):119-28.
- Bulloch B, Schubert CJ, Brophy PD, et al. Cause and clinical characteristics of rib fractures in infants. Pediatrics 2000; 105:E48.
- Barsness KA, Cha ES, Bensard DD, et al. The positive predictive value of rib fractures as an indicator of nonaccidental trauma in children. J Trauma 2003; 54:1107-10.
- Lonergan GJ, Baker AM, Morey MK, Boos SC. Child abuse: Radiologic-pathologic correlation. RadioGraphics 2003; 23:811-45.
- Barber I, Perez-Rossello JM, Wilson CR, Kleinman PK. The yield of high-detail radiographic skeletal surveys in suspected infant abuse. Pediatr Radiol 2015; 45:69-80.
- van Rijn RR, Sieswerda-Hoogendoorn T. Imaging child abuse: the bare bones. Eur J Pediatr 2012; 171:215-24.
- Mandelstam SA, Cook D, Fitzgerald M, Ditchfield MR (2003) Complementary use of radiological skeletal survey and bone scintigraphy in detection of bony injuries in suspected child abuse. Arch Dis Child 2003; 88:387-90.